No se puede tener un instrumental más «usado» que las micropipetas en un laboratorio de biología molecular. Dejando a parte el desgaste y mal uso, una correcta utilización asegura el buen rendimiento de las reacciones de PCR, por ejemplo, cómo utilizar las micropipetas sigue siendo un factor crucial en un laboratorio.
A parte de la elección de las puntas adecuadas (hay algunas que no se adhieren bien…y ya estamos en el problema del dinero y las marcas, pero no quiero meterme en eso ahora), la selección de la micropipeta para la medición seleccionada y de estar bien seguros de haber realizado las medidas previas correctamente, el problema está en el uso del émbolo.
Cómo utilizar las micropipetas Pasos
La ilustración siguiente explica lo que se suele enseñar (o por lo menos se enseñaba) en las prácticas de laboratorio:
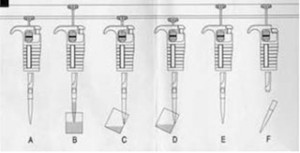
- Se aprieta el émbolo hasta el primer tope.
- Se introduce la punta y se aspira el contenido previamente ajustado en la micropipeta. Con cuidado de no generar burbujas.
- A la hora de verter el volumen aspirado, se aprieta hasta el primer tope.
- Presionar hasta el segundo tope para soltar el volumen completamente.
- Se desecha la punta en el recipiente correspondiente después de terminar.
Esto es lo que se suele aprender. Pero luego depende de las marcas y de cómo absorben los volúmenes. Incluso de las diferentes micropipetas dentro de la misma marca.
El dibujo, si se recuerda de cuando se daban prácticas, pertenece a unas micropipetas tipo Gilson. Algo rudas en su manejo, pero eficaces al fin y al cabo. Lo que quería saber y comentar es cómo las soléis usar. Así se puede aprender un poco y mejorar las técnicas. Veremos que existen muchas variantes sobre cómo utilizar las micropipetas .
Por ejemplo, en mi micropipeta de 12 canales se aconseja el uso en el manual de instrucciones. Allí se explica que lo mejor es apretar hasta el segundo émbolo y luego absorber el volumen resultante (previamente seleccionado el volumen, claro). Se vierte hasta el primer tope y , en las sucesivas pasadas, sólo se debe apretar hasta el primer tope y verter apretando siempre hasta el primer tope. Curioso esto del pipeteo ¿no?
Escuchando: Podcast número 15 de iCharlas

Me parece curioso porque ahora mismo estoy en ese dilema, hay gente que las usa vertiendo hasta el segundo tope, y otras hasta el primero, sobre todo por la cuestión de las burbujas. Además, algunas punteras también funcionan mejor que otras porque algunas retienen fluido tras varios «pipeteos».
Hola César. Lo de la retención del fluido tras varios pipeteos es cierto. A mi me ocurre con todas las micropipetas. Ahora utilizo las marcas Gilson y Finnpipette y tras utilizar las puntas, tanto de la misma marca como genéricas, en pipeteos masivos (como en placas multipocillos) terminan tomando ese volumen debido a la presión del fluido. Estas son pequeñas cosas que suceden en el laboratorio. Gracias por tu comentario.
Hola que tipo de ejercicio me pueden recomendar para las personas que recien se inician en el uso de estas micropipetas, estudiantes por ejemplo?
Pues se podrían hacer unos ejercicios simples, siempre después de haber practicado la teoría que expuse en el artículo. Con tubos de 1,5 ml, el profesor puede añadir volúmenes medidos y hacer que los alumnos vayan pasando a otros tubos cantidades inferiores. Suelo enseñar a mis alumnos que pipeteen con puntas finas (amarillas o transparentes, para volúmenes de unos 10 microlitros a 0,5 microlitros) y alojen los líquidos en las paredes de varios tubos de 0,2 microlitros. Así cogerán destreza, observarán el deslizamiento de los fluidos por las paredes de los tubos y comenzarán a controlar el pulso. Así también, como los volúmenes estarán medidos, se puede comprobar el posible error de pipeteo que ocurre en los ensayos y aprender así a ser conscientes de cómo preparar mezclas de reacción que luego añadir a diversas muestras.
Muchas gracias por el comentario, Carmen. Si necesitas algo más, aquí me tienes. Un saludo desde el lab 😉
Hola, solo para compartir mi experiencia, cuando hago PCR convencional y Real Time, uso la última técnica (absorber con los 2 tiempos y luego usar el primer tiempo) lo hago por el tema de las burbujas que pueden desnaturalizar la Taq-polimerasa y me va muy bien incluso se nota que la reproducividad tiene mayor precisión cuando calibro mi curva standard en el Real Time. Sin embargo me gustaría saber si alguien tiene un argumento coherente para no realizar ésta técnica de pipeteo, saludos.
Hola Víctor. Lo mejor es seguir las instrucciones del fabricante en primer lugar. Pero si usas un juego de micropipetas para tí (o para dos personas a lo sumo), la técnica es a gusto del consumidor y de para qué lo use. Yo he trabajado con micropipetas que al absorber volúmenes (tampoco muy elevados) apretando hasta el segundo tope la succión provocaba contaminaciones. Como lo lees. El deje de los investigadores a la hora de pipetear podría causar contaminaciones con volúmenes elevados fácilmente. Desde hace unos 6 años para acá, no he vuelto a ver problemas con micropipetas para volúmenes moderados. Es más, como comento en el artículo, ya has visto que yo también uso ese método con la multicanal.
Un abrazo y gracias por el comentario 😉
En que se dferencia los colores de plastico amarillo y rojo que se le coloca a la punta de una micropipeta.
Hola Grover. ¿Podrías ser más específico o, si puede ser, más gráfico?. Envía una imagen de lo que comentas porque no comprendo muy bien lo que explicas. Un saludo.
Hola! Qué dices de la inclinación de la micropipeta en el pipeteo? Aumenta el margen de error a diferencia si se realiza totalmente vertical o no?
¿Las puntas se pueden lavar? ¿Cuando llegan nuevas las puedo usar con toda la confianza? Gracias.
Hola, Elena. Lo más recomendable es que las puntas no se laven. Son fungibles diseñados para un sólo uso.
Cuando llegan nuevas, hay que leer el estado en el que las entregan. Si están estériles y tratadas o no con DNasas, por ejemplo. Lo mejor siempre es montar las cajas con las puntas y meter las cajas en una autoclave. Así también te aseguras de eliminar la posible contaminación por manipular las puntas. Recuerda que en un laboratorio la limpieza y esterilidad de las zonas y material de trabajo es esencial.
Espero que haya sido de ayuda. Un saludo .
Hola
gracias por compartir
independientemente de la calibración que se le haga a las micropipetas, se debe hacer alguna verificación por parte del analista? hay alguna recomendación?
saludos y gracias
Hola, tengo una pregunta. Adquirí una micropipeta para análisis microbiológico de leche fluida UHT con el fin de ir descartando el uso de pipetas de vidrio esterilizados. Las puntas vienen en bolsas plásticas de nuestro proveedor ya esterilizado, mi pregunta es, como manipular las puntas para colocar en la micropipeta sin el riesgo de contaminar las punteras con las manos..? Existen las famosas gradillas, pero no se tampoco la forma de uso o el tratamiento que se les da después de colocar las punteras en la gradilla y estar seguro que no se me haya contaminado por el manipuleo. Saludos
Hola.
luego de usar las micropipetas se deben guardar con un volumen marcado especifico o es aleatorio?
Hola,como haría el control de calidad de micropipetas
Ud. es el encargado de realizar el Control de Calidad en este caso clínico, explique como haría?
Indicador: El flebotomista reporta que el paciente hospitalizado carece de brazalete de identificación, por lo cual es difícil identificarlo.
Estándar: Todos los pacientes hospitalizados deben tener brazaletes para verificar su identificación.
ME PUEDE AYUDAR POR FAVOR
Holaaa .Disculpe quisiera saber cómo sería el correcto lavado de una puntera si en un laboratorio los quieren reciclar ???